血栓形成过程及常用 6 种抗血小板药物的作用机制
抗血小板聚集药物是脑梗死急性期、二级预防的主要治疗药物,它们通过作用于血栓形成的不同阶段,达到抗血小板聚集的作用。
本文对于临床常用的 6 种抗血小板药物的机制、药代动力学、出血等并发症处理、低反应性人群原因等问题进行梳理,以便于临床医生能够合理选择用药。
临床上抗血小板药物种类繁多,它们分别作用于血小板血栓形成过程中的不同阶段,抑制相关受体或酶,达到抗血小板的作用。主要集中在血小板血栓形成过程的粘附、聚集阶段。
血小板聚集形成血栓的过程
首先,我们来看看血小板聚集形成血栓过程的 5 个阶段。
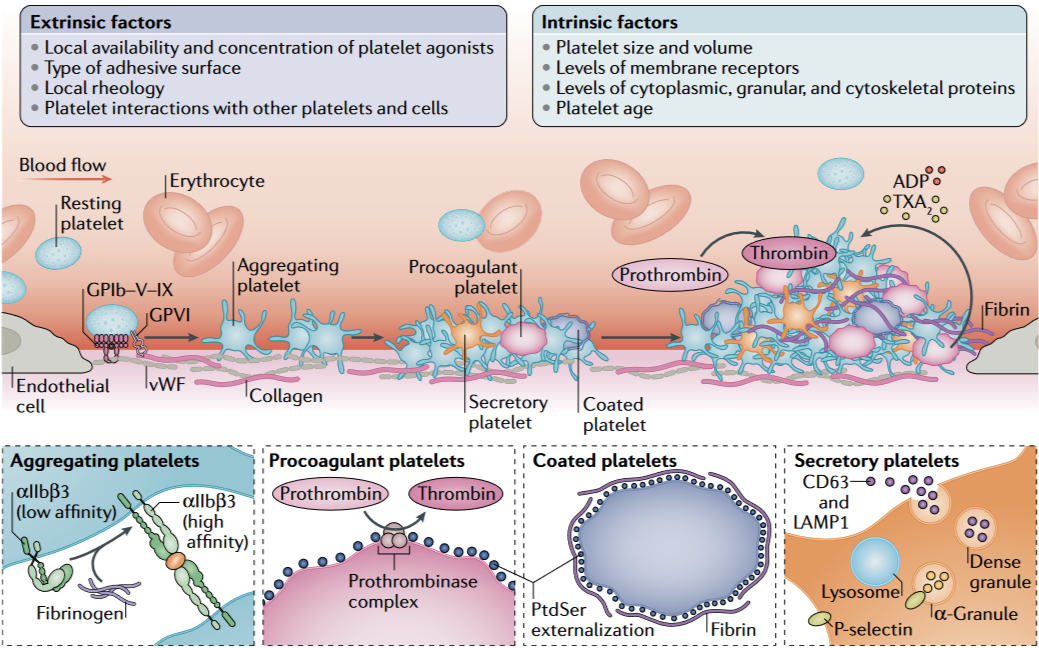
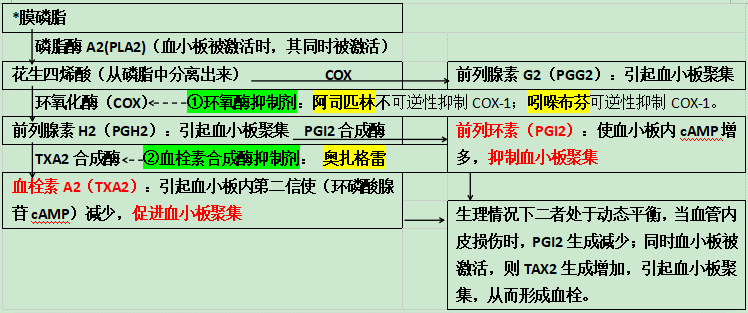
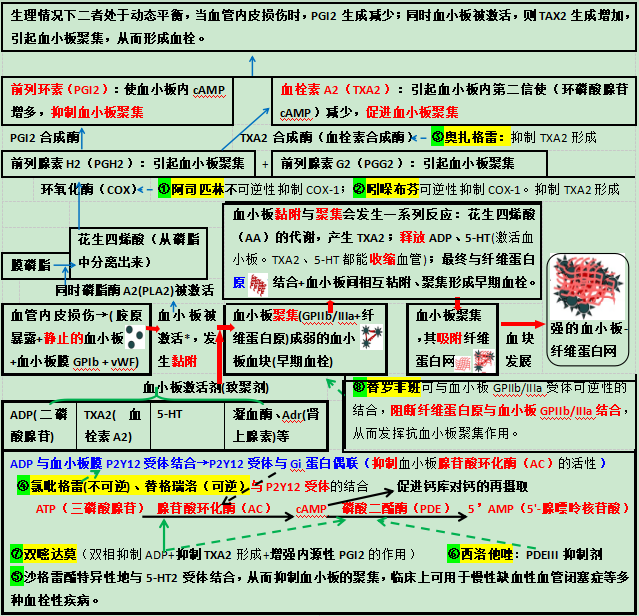
如下文中的图片所示,在细胞外基质(ECM),血小板表面的糖蛋白受体(GPVI,受体 GPVI)及 GPIb-IX-V 与血管内皮细胞释放的血管性血友病因子(vWF)等相互作用,导致血小板附着在胶原蛋白(collagen)上形成活化后的血小板。
随后,在整合素 αIIbβ3 的介导下,纤维蛋白原通过「桥联」的方式,两端与不同的 αIIbβ3 结合,最终导致血小板的聚集。激活的血小板还会释放内源性二磷酸腺苷(ADP)和血栓素 A2(TXA2),最终导致更多血小板的活化与聚集。
而上述机制中提到的相关分子,也就成了抗板药物的治疗靶点。
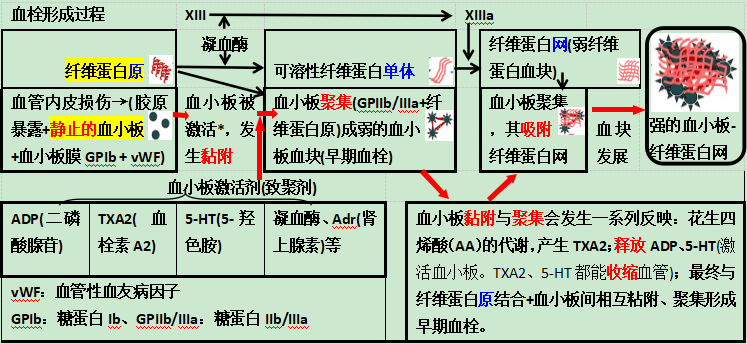
粘附:血管内皮损伤 → 胶原暴露 + 静止的血小板 + 血小板膜糖蛋白 Ib(GPIb)+ vWF(血管性血友病因子)→ 血小板被激活,发生黏附。
聚集:在血小板激活剂(致聚剂),如 ADP(二磷酸腺苷)、TXA 2(血栓素 A2)、5-HT(5-羟色胺)、凝血酶、Adr(肾上腺素)等作用下,血小板膜 GPIIb/IIIa 受体与纤维蛋白原结合成弱的血小板血块(早期血栓)。
释放:在血小板粘附与聚集过程中发生一系列反应:花生四烯酸(AA)的代谢,产生 TXA2;释放 ADP、5-HT 等。
血管收缩:TXA2、5-HT 能收缩血管。
吸附:血小板聚集,其吸附纤维蛋白网,血块发展为强的血小板-纤维蛋白网,即最终血栓形成。
血小板血栓形成过程与抗血小板药物的作用机制
接下来,我们来看看血小板血栓形成过程与抗血小板药物的作用靶点及机制。
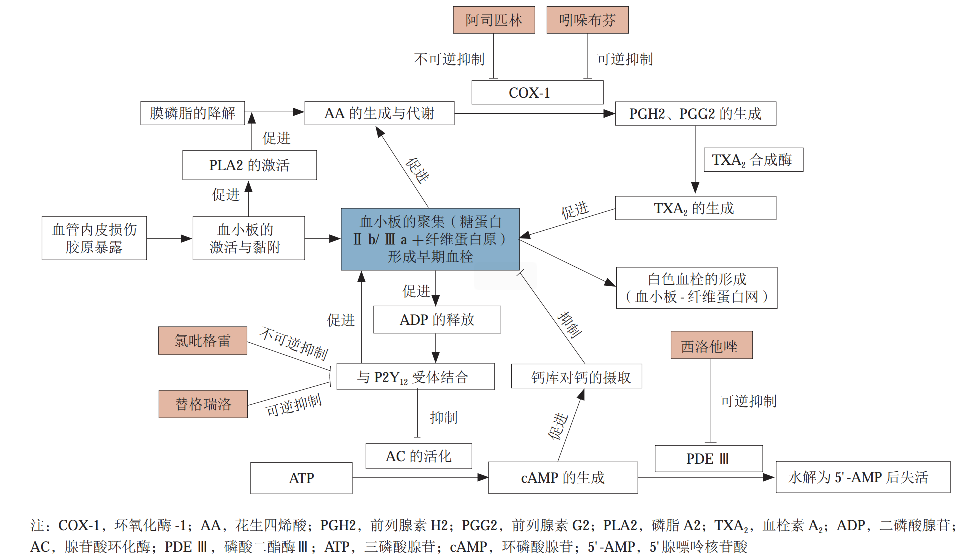
血小板被激活,黏附阶段
血小板聚集阶段

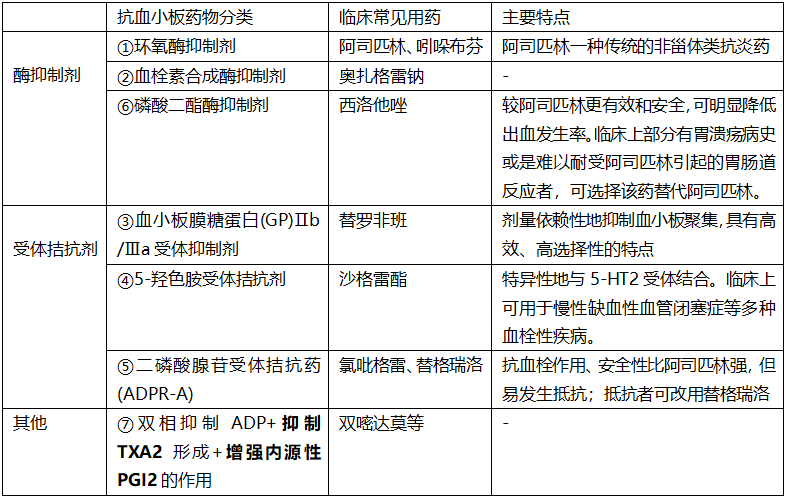
总结
6 种抗血小板聚集药物作用特点
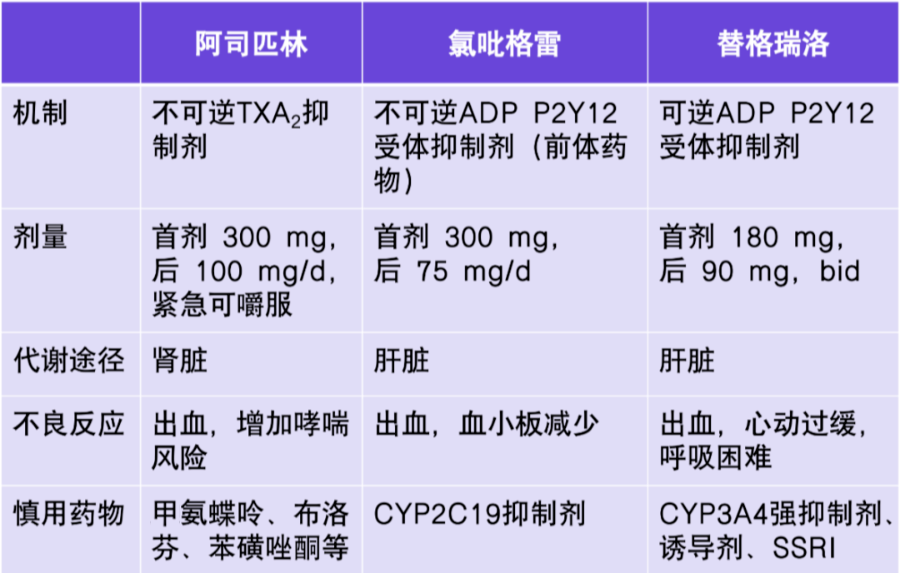
阿司匹林
机制:作为最经典的抗血小板药物,阿司匹林可以不可逆的抑制血小板环氧化酶(COX-1),导致 TXA2 生成减少,从而抑制血小板的聚集。
起效时间:阿司匹林的达峰时间约为 0.3~2 小时,清除半衰期与剂量相关;肠溶片较普通片吸收时间可延长 3~6 小时。因此,快速起效时可选择嚼服。
功能恢复时间:由于阿司匹林不可逆的抑制环氧化酶活性,因此,血小板功能的恢复需要等待血小板的再生,即完全停药后 7~10 天。
代谢途径:阿司匹林经由肾脏代谢,因此,使用时需考虑肾功能情况。禁用于合并氨甲蝶呤时,可能会减少其肾清除。
合并用药:同样作用于水杨酸的 NSAID,如布洛芬等,合并时也需要谨慎。此外,促进尿酸排泄的药物,如苯磺唑酮等,也可能需要谨慎。
注意事项:阿司匹林还可能导致支气管痉挛并引起哮喘发作,因此,也需要考虑患者是否合并哮喘。
服用时间:普通剂型的阿司匹林通常用于退热止痛,肠溶型的阿司匹林不会在酸性的胃肠道环境下溶解,而会进入碱性的环境,以尽量减少对胃肠道的刺激,因此,多建议餐前服用。
同时由于阿司匹林可以直接破坏消化道黏膜,其患者消化道出血的发生率远高于氯吡格雷。
氯吡格雷
机制:氯吡格雷经过 CYP450 酶代谢后,生成的活性代谢产物可以不可逆抑制 ADP 与血小板 P2Y12 受体的结合,从而抑制血小板的聚集。
起效时间:氯吡格雷的起效时间为 2~8 小时,由肝脏代谢,半衰期为 8 小时。
功能恢复时间:同阿司匹林类似,血小板正常功能的恢复速度与血小板的更新一致,约 7~10 天。
代谢途径:氯吡格雷部分经由肝脏代谢,经 CYP2C19 代谢为活性产物。根据已经鉴定的基因型,CYP2C19 基因通常被归类为超强代谢(*1/*17,*17/*17),快代谢(*1/*1),中等代谢(*1/*2,*1/*3)及弱代谢(*2/*2,*2/*3)。
因此,对于携带 *17 等位基因的患者,应该注意其出血风险;对于中等代谢的患者,可以考虑增加剂量或者换用其他药物;对于弱代谢的患者,可以考虑直接换用其他药物。
合并用药:由于氯吡格雷经由 CYP2C19 代谢,因此,应该避免与 CYP2C19 抑制剂合用,如:
质子泵抑制剂(奥美拉唑、埃索美拉唑)、抗真菌药(氟康唑、伏立康唑)、抗癫痫药(卡马西平、奥卡西平)、抗抑郁药(氟西汀、氟伏沙明、吗氯贝胺)、抗血栓药(氯苄吡啶)、抗组胺药(西咪替丁)以及抗生素(环丙沙星、氯霉素)。
患者如果需要使用质子泵抑制剂,可以使用泮托拉唑、兰索拉唑,也可使用除西咪替丁以外其他抑制胃酸分泌的药物。
替格瑞洛
机制:作为非噻吩吡啶活性药物,替格瑞洛可以可逆结合 P2Y12 抑制剂,从而抑制血小板的聚集。
起效时间:同氯吡格雷相比,替格瑞洛的起效时间更短,仅需 0.5~4 小时。
作用消失时间:作用消失时间也更短,仅需 3~5 天。
代谢途径:不同于氯吡格雷,替格瑞洛经由 CYP3A4 代谢,不受 CYP2C19 基因型的影响,因此,根据最新的 CHANCE-2 研究,可以作为对于 CYP2C19 等位基因缺失患者的替代治疗手段。
患者中重度出血事件的发生率与氯吡格雷类似,但总出血发生率高于氯吡格雷。
合并用药:与 CYP3A4 强抑制剂连用时应谨慎,包括抗真菌药物(酮康唑、伊曲康唑、伏立康唑)、抗生素(克拉霉素)、抗抑郁药(奈法唑酮)、抗病毒药(各种那韦)连用;
同时,也尽量避免与 CYP3A 诱导,如利福平、地塞米松、苯妥英钠、卡马西平及苯巴比妥连用;对于降脂药辛伐他汀及洛伐他汀,使用剂量不超过 40 mg;使用地高辛时应该注意监测;此外,尽量避免与 SSRI 连用,可能会增加出血风险。
不良反应:替格瑞洛具有呼吸困难的副作用,多发生于安静状态下;此外,替格瑞洛还可能出现室性心律失常,如心动过缓等;替格瑞洛可能会升高尿酸,因此,慎用于痛风患者。此外,替格瑞洛的出血风险相对高于氯吡格雷患者。
注意事项:替格瑞洛的使用为首剂 180 mg,此后 90 mg,bid,可以鼻饲。如患者漏服,下一次口服正常剂量即可。
替格瑞洛换用氯吡格雷时需要口服负荷量;反之,起始 180 mg 后,正常 90 mg,bid。
替罗非班
机制:作为非肽类血小板糖蛋白 IIb/IIIa 拮抗剂,替罗非班可以可逆性阻断血小板的交联及血小板的聚集。
临床应用:
非 ST 段抬高型急性冠脉综合征:
对于采用早期介入治疗策略且不准备在诊断后 4~48 小时内进行血管造影术的患者,首先予 0.4 μg/kg/min 静脉输注 30 分钟,继以 0.1 μg/kg/min 的速率持续静脉滴注。
经皮冠脉介入术:
对于计划在诊断后 4 小时内进行 PCI 的 NSTE-ACS 患者或计划进行直接 PCI 的 ST 段抬高型急性心肌梗死患者,应予 25 μg/kg 快速静脉推注,在 3 分钟内完成,继以 0.15 μg/kg/min 的速率维持静脉滴注 12~24 小时,最长可达 48 小时。
注意事项:目前替罗非班的适应证主要为用于心梗的治疗。现仅有注射用药,禁忌证为出血。
西洛他唑
机制:西洛他唑可以通过磷酸二酯酶活性使血小板内 cAMP 浓度上升,抑制血小板聚集,并可使血管平滑肌细胞内的 cAMP 浓度上升,使血管扩张,增加末梢动脉血流量。
注意事项:目前西洛他唑主要用于动脉硬化闭塞的治疗,现国内无注射用药,禁忌症为出血及充血性心衰。
用法:100 mg,bid。
双嘧达莫
机制:双嘧达莫可以通过抑制磷酸二酯酶活性使血小板内 cAMP 浓度上升,抑制血小板聚集,并可使血管平滑肌细胞内的 cAMP 浓度上升,使血管扩张,增加末梢动脉血流量。
此外,其还可以抑制血小板摄取腺苷、抑制 TXA2 以及增强内源性 PG1。
注意事项:禁忌症为出血;副作用为头晕、头痛、恶心、呕吐。
其他抗血小板药物
目前还有多种血栓素合成酶抑制剂奥扎格雷(仅有注射),前列环素受体激动剂贝前列素(多用于慢性闭塞),5-HT 受体拮抗剂沙格雷酯(用于慢性闭塞)。
近年来,糖蛋白 VI 抑制剂 Revacept、蛋白酶激活受体 1(PAR-1)沃拉帕沙、可逆性 COX-1 抑制剂吲哚布芬也逐渐引起人们的关注。
抗板药物的并发症及处理
在临床中经常可以遇到坚持抗板治疗作为二级预防用药,但是因为各种原因或无法耐受,仍反复发生血栓事件的情况。
出血风险及处理
出血是使用抗板药物的患者最常出现的副作用。年龄、高血压及肾功能不全将增加上述事件发生的风险。阿司匹林可以直接破坏消化道屏障,同时,不利于胃粘膜修复。
而同阿司匹林相比,吲哚布芬可以减少胃肠反应及出血风险,因此,可能可以作为对于阿司匹林不耐受患者的替代用药。西洛他唑也可以减少消化道出血的发生率,且联合用药没有增加出血性卒中风险,但由于其禁用于充血性心力衰竭,因此只能用于非冠心病患者。
尽管不会直接损伤消化道黏膜,P2Y12 抑制剂会阻碍溃疡愈合,因此,双联抗血小板药物治疗会严重增加消化道出血的风险。同氯吡格雷相比,替格瑞洛显著增加消化道出血的风险。
对于服用双联抗血小板药物同时有消化道出血病史或具有高危出血风险的患者,可合并使用质子泵抑制剂或者胃粘膜保护剂加 H2 受体抑制剂,也可使用吲哚布芬/西洛他唑合并氯吡格雷治疗。
如果患者已经出血,轻度出血无需停用抗血小板聚集药物;血红蛋白下降大于 30 g/L,但尚未引起血流动力学紊乱患者,可先停用阿司匹林;一旦出血停止,应该尽快恢复抗血小板治疗,3~5 天后恢复氯吡格雷,5~7 天后恢复阿司匹林,或者换为西洛他唑及吲哚布芬。
痛风
小剂量阿司匹林及替格瑞洛可引起血清尿酸水平增加及痛风复发,因此,慎用相关药物治疗。
抗血小板药物低反应性
抗血小板药物治疗低反应性通常指由于不同患者对同一种抗血小板药物的抗血小板作用反应不同,某些患者在治疗后血小板反应性仍较高(血小板功能检测提示血小板活性抑制不足),其发生血栓的风险显著增加。
**常见原因:多有遗传因素(COX-1 基因、P2Y12 受体基因多态性)、药物使用不规范(依从性差、剂量不足)、药物相互作用(如 NSAID 竞争性结合 COX-1)、合并症(高龄、肾功能不全、高血压)、血小板更新加速(手术、感染及出血)等。
对于高危缺血风险预后较差患者,建议进行基因检测及血小板功能检测,进一步明确原因,选择适合的药物。
版权声明
- 本文作者:Fermi
- 本文链接:https://fermi.ink/posts/2022/05/11/06/
- 转载标题:【转载】血栓形成过程及常用 6 种抗血小板药物的作用机制 —— Fermi
- 许可说明:本站所有文章除特别声明外均为博主原创作品,遵循 知识共享(CC BY-NC-SA 4.0)许可协议进行许可。非商业转载请注明原文出处(作者,原文链接)和本声明!商业转载请联系作者获得授权。
